Bayangkan sebuah benteng yang selama ini tidak bisa ditembus oleh obat-obatan MS konvensional. Benteng itu bernama Sawar Darah Otak (Blood-Brain Barrier). Selama bertahun-tahun, pasien dengan Multiple Sclerosis (MS) progresif sekunder hanya bisa melihat perkembangan kecacatan mereka berjalan terus, tanpa senjata yang cukup ampuh untuk menghentikannya dari sumbernya.
Namun, kabar baik datang dari uji klinis fase 3. Sebuah obat baru bernama Tolebrutinib, yang diklaim sebagai first-in-class BTK inhibitor oral, berhasil menembus benteng tersebut. Lebih dari itu, obat ini menghambat perkembangan kecacatan hingga 31% pada pasien MS progresif sekunder non-relaps (nrSPMS) . Bagi Anda atau keluarga yang hidup dengan kondisi ini, ini bukan sekadar berita riset; ini adalah secercah harapan baru di tengah keterbatasan pilihan terapi.

Mengapa Tolebrutinib Berbeda? Rahasia di Balik Sawar Darah Otak
Selama ini, sebagian besar terapi MS bekerja di “halaman depan” (sistem kekebalan perifer). Mereka efektif untuk MS relapsing, namun kurang optimal untuk MS progresif karena tidak bisa mencapai “ruang belakang” yaitu sistem saraf pusat (SSP).
Tolebrutinib berbeda. Ia dirancang sebagai brain-penetrant BTK inhibitor. Analoginya seperti ini: Obat lama hanya berperang di luar benteng, sedangkan Tolebrutinib diam-diam menyelinap masuk ke dalam markas musuh untuk melumpuhkan peradangan dari akarnya .
Dengan menghambat enzim Bruton’s Tyrosine Kinase (BTK), Tolebrutinib tidak hanya menekan sel B di darah tepi, tetapi juga menargetkan mikroglia—sel imun di otak yang bertanggung jawab atas peradangan kronis yang “membara” (smoldering neuroinflammation) dan menyebabkan kecacatan permanen .
Fakta Klinis: Angka 31% yang Mengubah Permainan
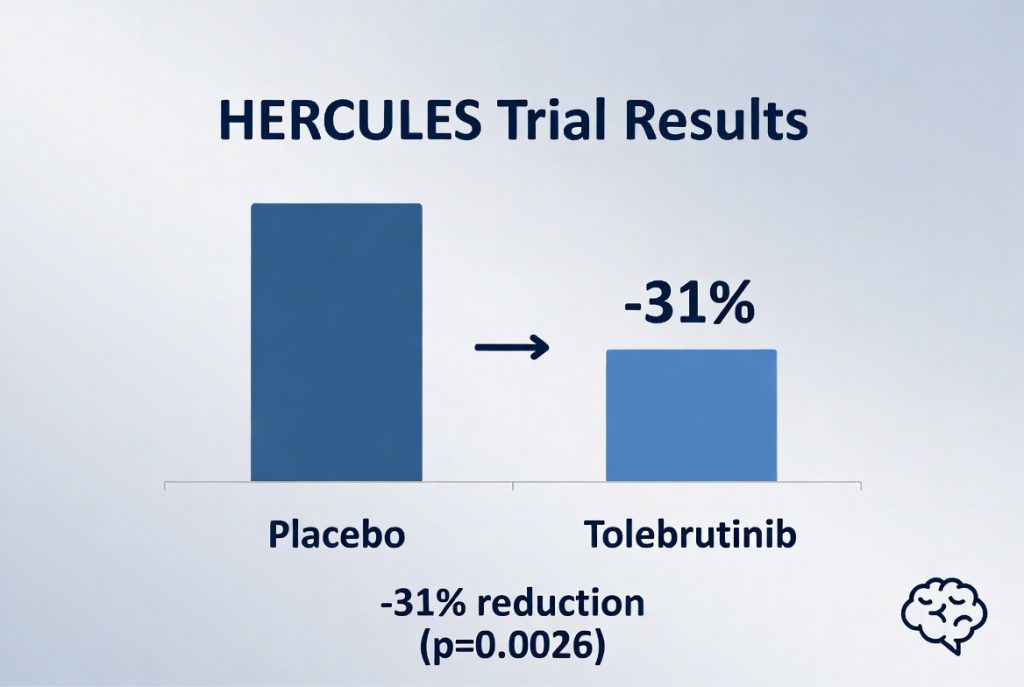
Data paling kuat datang dari studi HERCULES, yang hasilnya dipublikasikan di The New England Journal of Medicine (NEJM) pada April 2025.
Kutipan Studi: Studi ini melibatkan 1.131 partisipan dengan nrSPMS. Hasilnya menunjukkan bahwa mereka yang menerima Tolebrutinib memiliki risiko progresi kecacatan 31% lebih rendah dibandingkan plasebo (Hazard Ratio 0.69; P=0.0026) .
Tidak hanya berhenti di situ, studi juga menemukan bahwa pasien yang mengonsumsi Tolebrutinib 88% lebih mungkin mengalami perbaikan kecacatan (confirmed disability improvement) dibandingkan plasebo . Ini adalah insight penting: Obat ini tidak hanya memperlambat, tetapi dalam beberapa kasus, membantu perbaikan fungsi.
Dr. Robert Fox, ketua komite studi HERCULES dari Cleveland Clinic, menyatakan: “Ini adalah babak baru dalam MS, karena akhirnya kami menemukan cara potensial untuk mengobati bentuk MS progresif sekunder non-relaps.” .
Apakah Obat Ini untuk Anda? (Target Pasien)
Penting untuk dipahami bahwa Tolebrutinib secara spesifik ditujukan untuk Non-Relapsing Secondary Progressive MS (nrSPMS) .
- Kriteria: Pasien yang sudah tidak lagi mengalami relaps (serangan akut) setidaknya dalam 24 bulan terakhir, tetapi terus mengalami penumpukan kecacatan (semakin sulit berjalan, masalah kognitif, dll.) .
- Bukan untuk: Tolebrutinib terbukti tidak lebih unggul dalam menurunkan relapse rate dibandingkan terapi standar untuk MS relapsing .
- Catatan Penting (2026): Untuk MS progresif primer (PPMS), studi PERSEUS baru-baru ini diumumkan tidak memenuhi endpoint utama. Jadi, fokus utama obat ini tetap pada SPMS .
Yang Perlu Diwaspadai: Efek Samping dan Keamanan
Sebagai artikel yang baik, kami harus menyampaikan informasi baru yang jujur mengenai risiko. Efek samping yang paling menjadi perhatian adalah peningkatan enzim hati, yang merupakan karakteristik umum dari kelas obat BTK inhibitor.
Dalam studi HERCULES:
- Sekitar 4.0% pasien mengalami peningkatan enzim hati (ALT > 3x batas normal) dibandingkan 1.6% pada plasebo .
- Terdapat satu kasus fatal yang memerlukan transplantasi hati akibat komplikasi pasca operasi, yang terjadi sebelum protokol pemantauan ketat diterapkan .
Solusi untuk Pembaca: Jangan khawatir. Sanofi kini telah menerapkan protokol pemantauan hati yang ketat (tes darah rutin dalam 90 hari pertama). Dengan deteksi dini, hampir semua kasus peningkatan enzim hati dapat pulih tanpa intervensi medis lanjutan .
Status Ketersediaan dan Akses
Ini adalah kabar baik lainnya. Pada Agustus 2025, Tolebrutinib (nama merek CENRIFKI®) menerima persetujuan pertama di dunia di Uni Emirat Arab . FDA AS telah memberikan Priority Review dan diperkirakan akan mengumumkan keputusan resminya pada 28 September 2025 .
Meskipun mungkin belum tersedia di semua negara saat ini, kabar ini memberikan insight bahwa era pengobatan untuk MS progresif sudah di depan mata. Diskusikan dengan dokter saraf Anda apakah Anda memenuhi kriteria untuk nrSPMS dan apakah opsi ini atau uji klinis relevan untuk Anda.
Kesimpulan
Tolebrutinib membawa angin segar bagi komunitas MS progresif. Dengan kemampuannya menembus sawar darah otak, ia menawarkan solusi untuk hambatan kecacatan yang selama ini sulit diatasi. Meskipun ada tantangan terkait pemantauan fungsi hati, manfaatnya yang signifikan (31% hambatan progresi) menawarkan kualitas hidup yang lebih baik.
Call to Action: Simpan artikel ini. Bawa ke sesi konsultasi Anda berikutnya. Tanyakan pada dokter: “Apakah profil MS saya termasuk dalam kategori non-relapsing secondary progressive, dan apakah Tolebrutinib suatu saat nanti bisa menjadi pilihan untuk saya?”