Ivonescimab: Terobosan Antibodi Bispesifik yang Mengubah Standar Terapi
Selama ini, pasien kanker paru yang menjalani imunoterapi sering menghadapi dilema: efektivitas yang terbatas atau efek samping dari kombinasi dua obat terpisah. Namun, hadir sebuah terobosan dari China bernama Ivonescimab yang menawarkan pendekatan revolusioner. Berbeda dengan terapi konvensional yang memerlukan dua suntikan berbeda, Ivonescimab menggabungkan dua mekanisme sekaligus dalam satu molekul. Artikel ini akan membahas bagaimana obat kanker buatan China ini bekerja, seberapa efektif dibandingkan standar emas global, dan bagaimana aksesnya bagi pasien di Indonesia.
- Ivonescimab: Terobosan Antibodi Bispesifik yang Mengubah Standar Terapi
- Mengapa Terobosan dari China Ini Disebut Revolusioner?
- Data Klinis yang Mencengangkan: Mengalahkan Keytruda
- Manfaat Ganda yang Terkonfirmasi dari Uji Klinis
- Profil Keamanan: Efek Samping yang Terkendali
- Ketersediaan di Indonesia: Apa yang Bisa Dilakukan?
- Kesimpulan: Terobosan yang Mengubah Lanskap Pengobatan Kanker
- Referensi
Mengapa Terobosan dari China Ini Disebut Revolusioner?

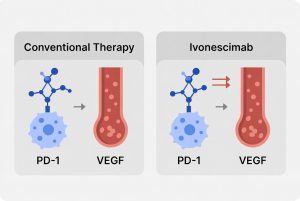
Ivonescimab (AK112) adalah antibodi bispesifik kelas pertama (first-in-class) yang dikembangkan oleh perusahaan bioteknologi China, Akeso, dan telah mendapat persetujuan dari otoritas obat China (NMPA) pada Mei 2024 [1]. Ia mampu menarget dua molekul kunci dalam perkembangan kanker secara bersamaan: PD-1 dan VEGF.
Agar mudah dipahami, bayangkan sistem imun Anda seperti pasukan keamanan tubuh. Kanker memiliki dua cara untuk meloloskan diri:
-
PD-1 adalah “rem” yang ditekan kanker agar pasukan imun berhenti menyerang.
-
VEGF adalah “pompa” yang mendorong pertumbuhan pembuluh darah baru untuk memberi makan tumor.
Ivonescimab bekerja dengan melepas rem dan mematikan pompa dalam satu suntikan. Yang menarik, penelitian menunjukkan bahwa ketika Ivonescimab mengikat VEGF, ikatannya dengan PD-1 justru menjadi lebih kuat menciptakan efek sinergis di mana 1 + 1 > 2 [2].
Data Klinis yang Mencengangkan: Mengalahkan Keytruda
Pertanyaan yang pasti muncul di benak pembaca: “Apakah terapi ini benar-benar lebih baik dari yang sudah ada?” Jawabannya, berdasarkan uji klinis fase 3 HARMONi-2 yang dipresentasikan di World Conference on Lung Cancer 2024, adalah ya, secara signifikan.
Dalam uji coba yang melibatkan 398 pasien dengan kanker paru non-sel kecil (NSCLC) stadium lanjut PD-L1 positif, Ivonescimab dibandingkan langsung dengan Keytruda (pembrolizumab) obat imunoterapi yang menjadi standar emas global. Hasilnya:
| Parameter | Ivonescimab | Keytruda |
|---|---|---|
| Median Progression-Free Survival (PFS) | 11,1 bulan | 5,8 bulan |
| Risiko Progresi atau Kematian | Turun 49% (HR 0,51) | – |
| Objective Response Rate (ORR) | 50% | 38,5% |
| Disease Control Rate (DCR) | 89,9% | 70,5% |
*Sumber: HARMONi-2 trial, dipresentasikan oleh Prof. Caicun Zhou dari Shanghai Pulmonary Hospital [3]*
“Ini adalah studi fase 3 pertama yang menunjukkan peningkatan efikasi yang signifikan secara klinis dengan obat baru dibandingkan pembrolizumab pada NSCLC lanjut,” ujar Prof. Zhou [3]. Keunggulan ini konsisten di semua subkelompok pasien, terlepas dari tingkat ekspresi PD-L1 atau jenis histologi tumor.
Untuk informasi lebih lanjut mengenai perkembangan terapi kanker terkini, Anda dapat membaca artikel kami tentang perkembangan imunoterapi terkini dan panduan memilih terapi target.
Manfaat Ganda yang Terkonfirmasi dari Uji Klinis
Tidak hanya pada terapi lini pertama, Ivonescimab juga menunjukkan hasil impresif pada pasien yang lebih sulit diobati: mereka dengan kanker paru non-skuamosa yang telah resisten terhadap terapi target EGFR-TKI.
Dalam uji HARMONi-A, dengan median follow-up 32,5 bulan, kombinasi Ivonescimab dengan kemoterapi menurunkan risiko kematian hingga 26% (HR 0,74) dan risiko progresi penyakit hingga 54% (HR 0,46) dibandingkan kemoterapi saja [4]. Data ini membuat HARMONi-A menjadi studi imunoterapi fase 3 pertama di dunia yang melaporkan manfaat positif untuk overall survival dan progression-free survival secara bersamaan pada populasi yang sulit ini.
Berdasarkan data tersebut, pada November 2024 Ivonescimab resmi masuk dalam daftar obat nasional China (NRDL) sehingga lebih mudah diakses pasien [4].
Profil Keamanan: Efek Samping yang Terkendali
Kekhawatiran umum tentang terapi baru adalah efek samping. Pada uji HARMONi-2, efek samping terkait pengobatan derajat 3 atau lebih berat terjadi pada 29,4% pasien yang menerima Ivonescimab. Angka ini sebanding dengan terapi kombinasi konvensional. Yang membedakan, efek samping yang lebih sering muncul adalah proteinuria (kelebihan protein dalam urine) dan hipertensi khas dari penghambat VEGF namun secara umum dapat dikelola [3].
Yang patut dicatat, tidak ada efek samping imun terkait yang menyebabkan penghentian pengobatan, dan hanya 1,5% pasien yang menghentikan Ivonescimab karena efek samping [3].
Untuk memahami lebih dalam tentang manajemen efek samping terapi kanker, kunjungi halaman tips mengelola efek samping imunoterapi.
Ketersediaan di Indonesia: Apa yang Bisa Dilakukan?
Pertanyaan paling praktis: “Apakah terapi ini sudah tersedia di Indonesia?”
Saat ini, Ivonescimab telah mendapat persetujuan di China dan sedang dalam evaluasi global untuk berbagai tumor padat [2]. Untuk pasien di Indonesia yang tertarik, beberapa opsi dapat dipertimbangkan:
-
Konsultasi dengan Onkolog: Dokter spesialis dapat mengevaluasi apakah profil genetik dan kondisi pasien sesuai dengan indikasi Ivonescimab.
-
Uji Klinis: Pantau apakah ada uji klinis fase lanjut yang membuka rekrutmen di Indonesia melalui situs ClinicalTrials.gov.
-
Medical Tourism: Beberapa pasien memilih berobat ke China atau Singapura di mana terapi ini telah tersedia dengan pengawasan medis yang ketat.
Menurut laporan dari World Health Organization, akses terhadap terapi inovatif terus berkembang seiring dengan peningkatan kerja sama regional di Asia Tenggara.
Kesimpulan: Terobosan yang Mengubah Lanskap Pengobatan Kanker
Ivonescimab bukan sekadar obat baru. Ia adalah bukti bahwa pendekatan bispesifik menyatukan dua mekanisme dalam satu molekul dapat memberikan hasil yang lebih baik dengan efisiensi lebih tinggi. Dengan data yang menunjukkan superioritas terhadap Keytruda di lini pertama dan manfaat survival yang jelas pada pasien resisten, para ahli seperti Dr. John Heymach dari MD Anderson Cancer Center menyebutnya sebagai “kemungkinan standar perawatan baru” di masa depan [2].
Bagi pasien dan keluarga yang sedang berjuang melawan kanker, kehadiran Ivonescimab membawa harapan baru: terapi yang lebih efektif, dengan satu suntikan, dan akses yang semakin luas.
Langkah selanjutnya? Diskusikan dengan dokter onkologi Anda apakah terapi berbasis PD-1/VEGF ini relevan dengan kondisi Anda. Dunia pengobatan kanker bergerak cepat dan terobosan seperti Ivonescimab adalah alasan untuk tetap optimis.
Referensi
-
National Medical Products Administration (NMPA). Ivonescimab Approval Summary. 2024.
-
Herbst R, Chen L. The evolving immuno-angiogenic paradigm in NSCLC: lessons from ivonescimab. Nature Reviews Clinical Oncology. 2025;22:461-462. PMID: 40329050. Tersedia di: Nature.com
-
Zhou C, Chen J, Wu L, et al. Phase 3 study of ivonescimab (AK112) vs pembrolizumab as first-line treatment for PD-L1-positive advanced NSCLC: Primary analysis of HARMONi-2. 2024 World Conference on Lung Cancer. Abstract PL02.04.
-
Akeso, Inc. Ivonescimab’s Updated Label Shows Positive Dual Results in PFS and OS from HARMONi-A Study. 2026.